2.4 Energiezufuhr und Aggregatzustandsänderung
Im Kapitel 2.2 hast bereits erfahren, dass Stoffe in drei Aggregatzuständen vorkommen und ihren Aggregatzustand ändern können. Hier wirst du dein Wissen darüber vertiefen.
Zuerst aber kommt die Lösung zu der Hausaufgabe "Versuch mit dem Tee und seine Deutung". Vergleiche mit deiner Lösung und korrigiere!
In dem Glas mit dem heißen Wasser breiten sich die Teeteilchen schneller als im kalten Wasser. Da die Ursache für die Durchmischung die Bewegung von Wasser- und Teeteilchen ist, müssen sich die Teilchen vom heißen Wasser schneller bewegt haben, als die Teilchen vom kalten Wasser.
Die Bewegung der Teilchen eines Körpers und seine Temperatur hängen also zusammen:
Je schneller sich sich Teilchen bewegen, desto höher ist die Temperatur des Körpers.
In der Luft bewegen sich die Teilchen so schnell, dass sie nazu Schallgeschwindigkeit haben. Aber sie sind nicht alle gleich schnell. Es gibt in jedem Körper einige, die sich schneller bewegen, und einige, die langsamer sind. Deshalb lässt sich nicht die Geschwindigkeit einer einzelnen Teilchens angeben, sondern immer nur ein Mittelwert für alle.
Damit ist nun auch verständlich, wo beim Erhitzen oder Reiben zugeführte Energie geblieben ist: Da sich die Teilchen bewegen, haben sie Bewegungsenergie. Bei Energiezufuhr nehmen sie Energie auf und wandeln sie in Bewegungsenergie um. Insgesamt wächst dadurch ihre Bewegungsenergie, sie bewegen sich schneller, die Temperatur des Körpers steigt.
Was geschieht beim Abkühlen eines Körpers?
Der Körper gibt Energie ab. Die Teilchen werden langsamer, weil ihre Bewegungsenergie abnimmt, die Temperatur des Körpers sinkt. Führt man diesen Energieentzug immer weiter, so müssen schließlich alle Teilchen zur Ruhe kommen, wenn sie ihre gesamte Bewegungsenergie abgegeben haben (Erstarren). Genaue Messungen zeigen, dass das bei -273,15°C der Fall ist. Niedrigere Temperaturen kann es nicht geben, denn noch mehr energie können Teilchen nicht verlieren. Deshalb wurde diese tiefste erreichbare Temperatur als Nullpunkt auf die Kelvin-Temperaturskala gewählt:
-127,15°C=0 K sind absolute Nulpunkt.
Temperatur eines Körpers ist ein Maß für die Bewegungsenergie seiner Teilchen.
Wenn Eis von 0°C Energie zugeführt wird, dann erhöht sich seine Temperatur zunächst nicht, sondern es wird zu Wasser, es schmilzt. Energiezufuhr führt also nicht immer zu Temepratursteigerungen, sondern lann auch eine Änderung der Zustandsform bewirken. Durch Energiezufuhr wird dabei der Zusammenhalt zwischen den Teilchen geändert: Sie schwingen heftiger und verlassen schließlich ihren Platz im Gitter-aus dem festen Körper ist eine Flüssigkeit geworden (Schmelzen). Erst wenn sich im gesamten Körper die Bindungen zwischen den Teilchen gelöst haben, steigt die Temperatur (jetzt im Wasser) bei weiterer Energiezufuhr wieder an.
Der Zusammenhang zwischen Energiezufuhr und Zustandsänderung ist hier in einem Diagramm dargestellt:
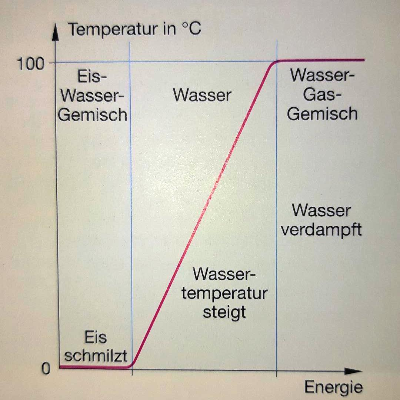
Ähnliches geschieht beim Verdampfen, wenn die Flüssigkeit gesförmit wird: Die Temperatur bleibt konstant, weil alle zugeführte Energie zum völligen Lösen der Bindungen zwischen den Teilchen gebraucht wird.
WERDE AKTIV 1
Zeichne in Anlehnung an Abb. 1
a) ein beschriftetes Energie-Temperaturdiagramm für den Übergang zwischen dem flüssigen und gasförmigen Zustand beim Wasser (Verdampfen) und
b) ein beschriftetes Energie-Temperatur-Diagramm für den Übergang zwischen einem festen und einem flüssigen Zustand beim Wassers (Schmelzen) und reiche ein.
Temperaturänderung ohne Energiezufuhr?
Eispacks sind Kühlaggregate, die man allerdings nur einmal nutzen kann. Die löst man aus, indem man sie zusammenquetscht. Man nutzt sie zum Kühlen von Getränken, aber vor allem auch zur Behandlung von Sportverletzungen.
Wie funktionieren sie?
Aufgetrenntes Eis-Pack

Wir aktivieren ein Eispack, indem wir entsprechend der Vorschrift draufdrücken. Die Flüssigkeit vermischt sich mit den deutlich fühlbaren Kügelchen. Sofort beginnt das System, sich stark abzukühlen.
Wenn du möchtest und eine Möglichkeit dazu hast, kannst du ein Versuch selbst durchführen!
Versuch mit dem Kühlpack
Entgegen der Aussage im Film kannst du den Versuch freiwillig nachmachen!
Öffne vorsichtig ein Kühlpack, mische in einem Becherglas (25 ml) 5 g der Kügelchen und 5 g Flüssigkeit, deren Temperatur du zuvor gemessen habst. Am besten nimmst du dazu ein elektronisches Thermometer. Dann gib beide Substanzen zusammen und rühre um. Die Temperatur sinkt beim Test innerhalb ein-zwei Minuten von 20,4 auf -0,2 °C. Während der Temperaturmessung gut umrühren!
Erklärung
Es ist tatsächlich ein Eispack! Was ist da passiert?
Vielleicht gibt uns die auf der Packung angegebene Zusammensetzung Hinweise. Der Inhaltsstoff Kalkammonsalpeter (Salz) wird mit dem Wasser vermischt, Das Salz löst sich im Wasser auf.
Dabei kühlt sich die Mischung ab, weil Energie benötigt wird, um die Salzteilchen aus dem festen Verbund des Kristallgitters auszulösen. Da von außen keine Energie zugeführt wird, kann sie nur den Wasser- und Salzteilchen entzogen werden. Dadurch vermindert sich die Bewegungsenergie, was eine Temperaturabnahme zur Folge hat.
WERDE AKTIV 2
Finde heraus wie ein Wärmepack funktioniert und erkläre was passiert aus energetischer Sicht.
Anteile der inneren Energie

Übertrage das Diagramm und den Text in dein Heft:
In der Abbildung 2 ist dargestellt aus welchen Anteilen innere Energie besteht:
1. Bewegungsenergie der Teilchen. Sie kann verändert werden, indem man Energie von außen zuführt oder dem Körper entzieht. Dieser Anteil ist also veränderbar.
2. Energie, die zum Zusammenhalt der Teilchen untereinander benötigt wird. Diser Energieanteil ist dafür verantwortlich, welchen Aggregatzustand der betreffender Körper hat. Durch Zufuhr oder Entzug von Energie kann dieser Energieanteil verändert werden, was zu den bekannten Änderungen der Zustandsformen "Schmelzen", "Verdampfen", " Kondensieren" oder "Erstarren" führt.
3. Chemische Energie, die in den Bindungen verschiedener Teilchenarten aneinander steckt, z. B. die Bindung zweier Wasserstoff- an ein Sauerstoffatom beim Wasser (H2O). Außerdem gehört dazu die Kernenergie, die die Atome in sich zusammenhält (Elementarteilchen Elektronen in der Atomhülle, sowie Protonen und Neutronen im Kern).
